Тимома – доброкачественное или злокачественное новообразование вилочковой железы, которое при несвоевременном лечении может привести к серьезным осложнениям. У ¾ пациентов тимомы имеют доброкачественный характер, тогда как у ¼ – злокачественный. Деление на доброкачественные и злокачественные производится в зависимости от внешнего вида, степени дифференциации пораженных клеток и их склонности к распространению. Тимомы встречаются крайне редко как у взрослых, так и у детей.
Содержание
Что такое тимома?
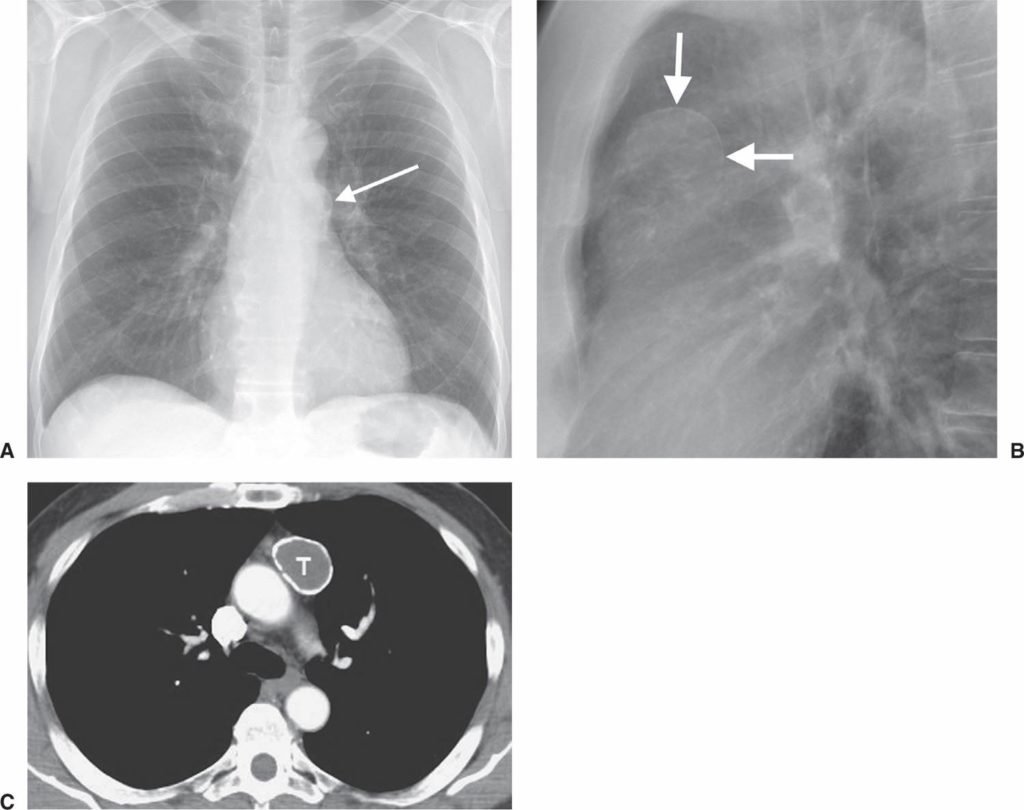
Тимомы встречаются преимущественно у людей старше 30-40 лет (опухоли у детей встречаются очень редко)
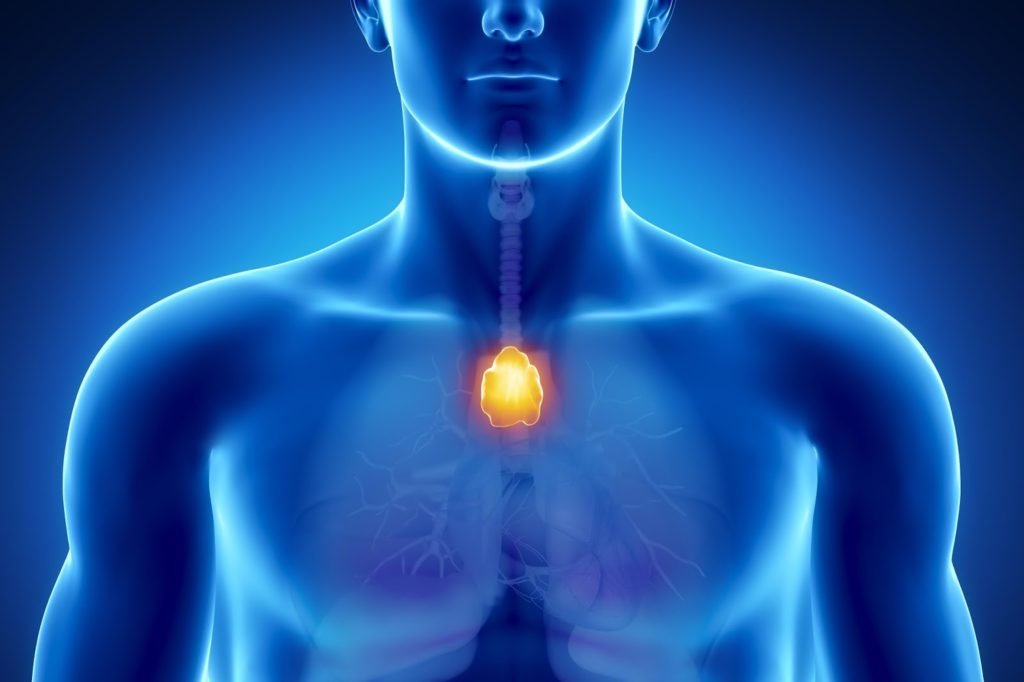
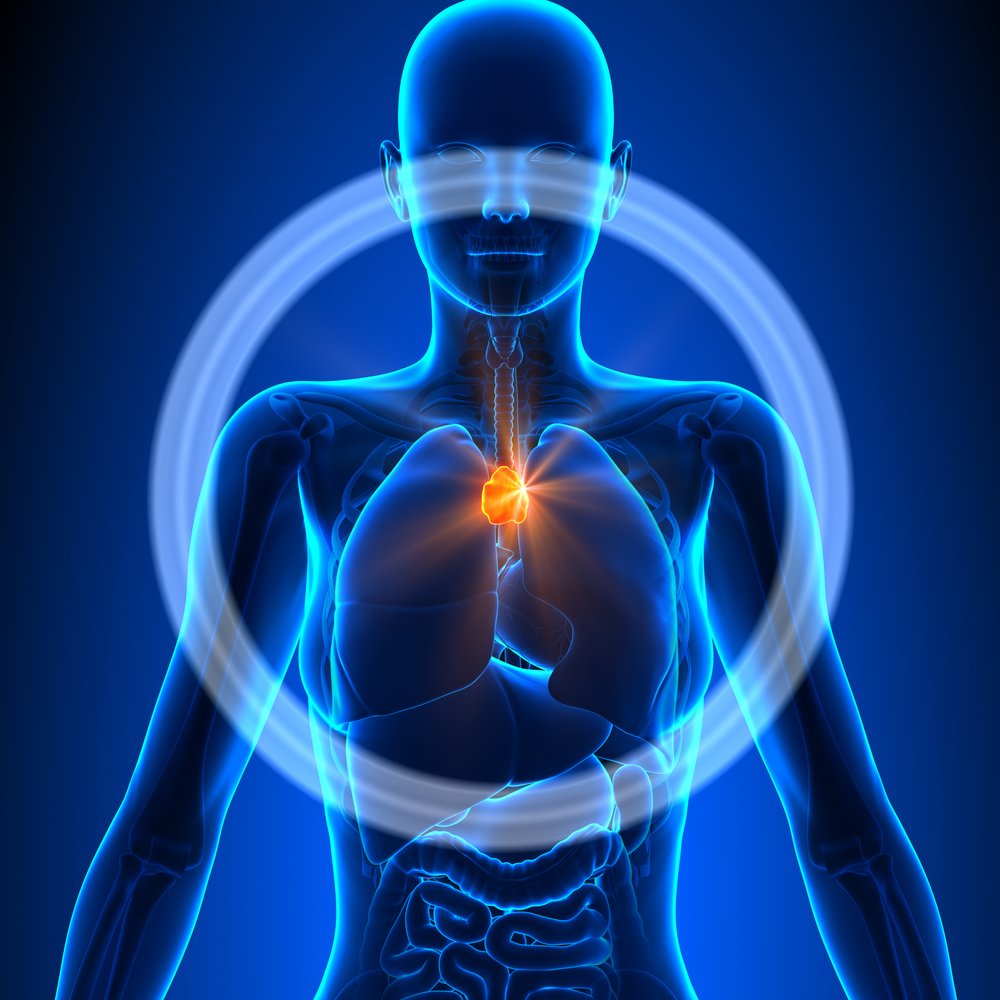
Тимус – орган лимфопоэза, расположенный в переднем средостении, который был описан Галеном в Древней Греции; он считал его местом пребывания души. Тимус состоит из двух долей, соединенных вместе. Тимус растет с рождения до полового созревания, а затем постепенно уменьшается в размерах.
Тимус специализируется на созревании определенных лимфоцитов – клеток иммунной системы – ответственных за распознавание и уничтожение чужеродных клеток. Эпителиальное пространство тимуса в основном состоит из лимфоцитов (также называемых тимоцитами), а также некоторых эпителиальных и мезенхимальных клеток. В основном из эпителиальных клеток образуются тимомы.
Только в начале XX века начали изучать болезни вилочковой железы. Отношения между тимомами и миастенией – заболевание, характеризующееся мышечной слабостью – были описаны в 1901 г. немецким неврологом Германом Оппенгеймом. Врач обнаруживал при посмертном вскрытии пациентов с миастенией опухоли вилочковой железы (тимомы). В том же году немецкий патологоанатом Карл Вейгерт описал гистологические особенности одной из этих опухолей. Потенциальный метастатический характер был отмечен в 1905 году Эдуардом Фаркуаром. В 1900 году термин «тимома» впервые был использован Фридрихом Вильгельмом. Этот термин первоначально охватывал все опухоли тимуса, независимо от их точного характера.
Опухоли в области вилочковой железы встречаются с одинаковой частотой как у мужчин, так и у женщин. Если у пациента миастения, тимома обычно появляется в возрасте от 30 до 40 лет; если ее нет – в возрасте от 60 до 70 лет. Опухоли встречаются очень редко у детей.
Не существует известного фактора риска, который бы увеличивал риск развития тимомы. Наследственный характер тимомы встречается редко и связан с хромосомной транслокацией. Не существует никакого вирусного фактора, который напрямую увеличивает риск развития опухоли в области вилочковой железы.
Классификация
В онкологической практике различают 2 типа тимом: доброкачественные и злокачественные. Выделяют 4 стадии развития тимомы:
- I стадия: тимома ограничена тимусом;
- II стадия: злокачественное новообразование прорастает в медиастинальную клетчатку;
- III стадия: опухоль прорастает в легкое, перикард, крупные сосуды или плевру;
- IV стадия: возникают гематогенные или лимфогенные метастазы.
Симптомы

Наиболее распространенный симптом – боль в грудной клетке, которая может отдавать в шею, плечо, между лопатками
Тимома часто протекает бессимптомно: от 1/3 до ½ пациентов не имеют клинических признаков. В большинстве случаев опухоль тимуса выявляется случайно в ходе обследований по другим причинам.
Проявления болезни (кашель, боль в груди, трудности при глотании и одышка), связанные с массовым воздействием на внутригрудные органы, возникают у 40% пациентов. Около 30% пациентов имеют общую симптоматику – усталость, слабость, головную боль, потерю веса – которая может спонтанно исчезать.
Причины
Опухоль в области вилочковой железы чаще всего встречаются изолированно. Тем не менее, тимомы могут сопровождаться паранеопластическим синдромом – этот термин охватывает все аномалии, которые могут сопровождать определенные опухоли. Аномалии напрямую не связаны с опухолью, но являются проявлениями, происходящими на расстоянии от места, где развивается рак. Это редкие синдромы, которые обычно не встречаются при тимомах.
Миастения гравис – аутоиммунное нервно-мышечное заболевание. Миастения характеризуется нарушением передачи нервно-мышечных сигналов, что приводит к чрезмерной утомляемости поперечнополосатых мышц.
От 15 до 20% пациентов с раком в области вилочковой железы также имеют клинические признаки миастении, а 25% пациентов – антитела против ацетилхолинового рецептора (антитела против ACh-R). Любой носитель тимомы, демонстрирующий признаки миастении, будет иметь положительные антитела.
Диагностика
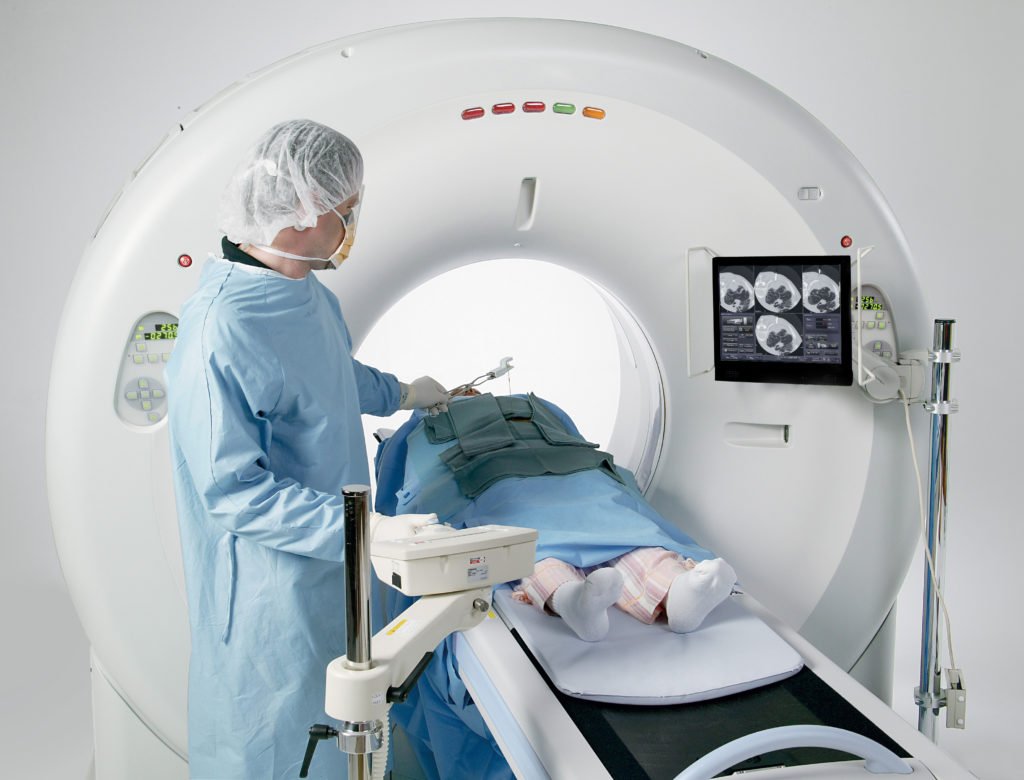
Для диагностики опухоли вилочковой железы используется компьютерная томография или магнитно-резонансная томография (МРТ используется реже)
В большинстве случаев достаточно проведения клинических и радиологических обследований тимуса. Рентгенограмма грудной клетки позволяет выявить у 45%-80% пациентов рак тимуса. Рентгенография средостенных органов – метод выбора при подозрении на злокачественные или доброкачественные тимомы.
Торакальная КТ более точная диагностическая процедура, чем рентгенография грудной клетки. В этом случае инъекция йодированной контрастной среды не всегда необходима, но помогает выявить вовлечение других органов. Тимомы выглядят на КТ как четко выраженная масса, расположенная вблизи перикарда. Масса может быть сферической или дольчатой, но имеет однородный вид (реже кистозный), который хорошо визуализируется с помощью контрастного вещества.
МРТ редко используется в диагностике злокачественного заболевания (онкологии тимуса), но может быть полезна в некоторых случаях. Пациент, который не может получить инъекцию контрастных средств, может извлечь пользу из МРТ. Обследование также может помочь дифференцировать средостенную кисту от злокачественной тимомы.
Диагноз подтверждается путем биопсии (взятия образца ткани для микроскопического анализа). Биопсия также требуется для дифференциации тимомы и лимфомы, поскольку лечение этих болезней различается. Рак тимуса должен исследоваться только квалифицированным патологоанатомом.
При необходимости биопсию можно выполнить несколькими способами. Хирургические биопсии (в основном, с помощью медиастинотомии) позволяют установить рак в области вилочковой железы в 90% случаев, но требуют общей анестезии. Биопсия под контролем КТ не требует общей анестезии и менее инвазивна, но позволяет диагностировать только в 60% случаях тимому. Выбор метода производится в соответствии с доступностью опухоли и общим состоянием пациента.
Дифференциальная диагностика проводится с другими доброкачественными опухолями – эктопический зоб, аденома паращитовидной железы, тимолипома или тератома. Также возможно сосудистое происхождение (аневризма) новообразования. В других случаях увеличение вилочковой железы могут имитировать опухоли, которые не происходят из тимусной ткани – лимфосаркомы.
Лечение
Тимомы в большинстве случаев являются доброкачественными опухолями, которые развиваются очень медленно. Однако с течением времени они могут вырождаться в рак тимуса.
Дополнительное лечение зависит от того, в какой степени рак в области вилочковой железы распространился на окружающие ткани. Хотя большинство случаев доброкачественны и требуют только хирургического вмешательства, инвазивные опухоли обычно требуют послеоперационной лучевой терапии, чтобы уменьшить вероятность рецидива. Опухоли, которые распространились на легкие и сердце, могут потребовать химиотерапии в дополнение к хирургии и радиотерапии. В большинстве случаев тимомы не уменьшают продолжительность жизни пациента при своевременно начатом лечении.
Оперативное вмешательство
Основной метод лечения – хирургическое удаление тимомы, чем раньше выполнена операция, тем больше шансов на выздоровление
Первичной терапией рака является полная хирургическая резекция вилочковой железы, особенно на ранних стадиях. Некоторые авторы считают, что неполная резекция, сопровождаемая адъювантной лучевой терапией и химиотерапией, может быть более эффективной, чем полное удаление тимуса.
Используются два основных хирургических подхода: стернотомия («трансцернальная тимэктомия») и видеохоракоскопия («тиреотомия с видео», которую может выполнять робот). Также используются малоинвазивные подходы – медиастиноскопия. Выбор подхода осуществляется в соответствии с характеристиками тимомы.
Химиолучевая терапия
Адъювантная терапия представляет собой химиотерапию или лучевую терапию, выполняемую после операции, чтобы уменьшить риск рецидива. Неоадъювантная терапия используется перед операцией, чтобы уменьшить размер опухоли.
Хотя тимомы обычно хемочувствительны даже на поздних стадиях развития, современных научных данных об эффективности химиолучевой терапии не существует. На ранних стадиях хирургическое вмешательство остается стандартным лечением и может быть дополнено адъювантной терапией. На более поздних стадиях рекомендуется оперативное вмешательство с химиолучевой терапией.
Прогноз
5-летняя выживаемость после хирургической резекции составляет около 85%, даже для пациентов с запущенными стадиями заболевания. Общая 15-летняя выживаемость составляет 70% на ранних стадиях. Долгосрочное выживание имеет тенденцию к увеличению с 1980-х годов, в связи с более ранней диагностикой и появлением новых хирургических методов.
Причина смерти пациентов связана с тимомой в 19-58 % случаях. В 2-19% случаях пациенты умирают от осложнений после операции, а в 16-27 % – от миастении. Около 90% рецидивов сопровождаются плевральными метастазами. Некоторые гистологические типы имеют более высокий риск рецидива после лечения. Стадия при постановке диагноза также является прогностическим фактором рецидива.
Из-за позднего начала лечения частота рецидивов может быть намного выше. Рекомендуется ежегодно проводить обследования и отслеживать концентрацию биомаркеров опухоли в кровеносном русле.